基于投资博腾股份的需要,我们一直在跟踪下全球瑞德西韦的研发进度,我们还连写整理了一份瑞德西韦的专题研究报告,在个人公号【复利无声】《瑞德西韦中国临床试验真的失败了吗?》,有兴趣的朋友,可以移步查看。$博腾股份(SZ300363)$
《新英格兰医学杂志》首次发布瑞德西韦同情用药的回顾性分析结果
4月11日,吉利德在《新英格兰医学》杂志上发布了瑞德西韦治疗新冠肺炎的首个同情用药临床研究结果。结果显示,在53名来自美国、欧洲、加拿大及日本的严重和危重新冠肺炎患者中,瑞德西韦给68%(36人)的患者带来临床改善。其中,57%(30/53)接受机械通气的患者中有17例已拔管。共有47%(25/53)的患者出院,13%(7/53)患者死亡;在接受有创通气的患者中,死亡率为18%(6/34),而未接受有创通气的患者为5%(1/19)。
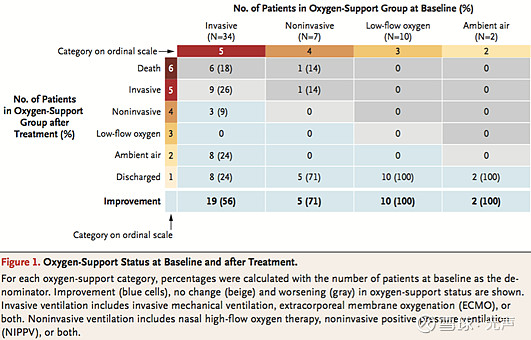
点评:这是首次公布瑞德西韦同情用药的多个病例回顾性分析结果,但没有设计对照组,类似于医生的个人临床经验观察总结,不能下明确结论,只能说初步看起来有效。
中国开展的两项临床试验已提前终止,重症组相关的结果有望于近期公布
针对中国两项临床试验的最新进展,吉利德方面4月16日中午在一份独家回应第一财经记者的声明中称:“我们被告知,由于入组人数低,由中国研究机构牵头的瑞德西韦针对新型冠状病毒肺炎重症患者和轻中症患者的两项临床研究已提前终止。”吉利德公司还表示:“我们期待着这些数据的发表和对结果的深入评审。”第一财经记者从多方了解到,尽管瑞德西韦中国的临床试验宣布停止,但是重症组已经收集到有效数据,相关的结果有望于近期公布。4月12日,试验负责人曹彬教授在一场线上访谈中透露,目前重症试验的临床数据正在分析中。
吉利德公司主导的两项临床试验将于5月结束
2月26日,吉利德公司宣布在全球启动两项瑞德西韦临床试验,均为随机、开放标签、标准治疗对照的临床试验。开放标签意味着对研究者和受试者都不设盲,试验过程中双方都知道真实的用药情况,因而不同于随机双盲试验。两组试验分别原计划入组400例重症患者和600例中症患者。4月9日,吉利德扩大两项临床试验入组人数,其中重症患者数量由400人增加至2400人。4月17日,吉利德再次扩大了重症患者的招募数量,由最初的2400人扩大至6000人,轻症患者数量为1600人。病患数量的增加有助于吉利德公司收集更多数据,以充分证明瑞德西韦药物的有效性。而据负责美国芝加哥大学临床试验的传染病学家凯瑟琳·马兰介绍,吉利德公司将于4月17日“锁定(locked)”重症临床试验最初入组的400名受试患者的数据,这意味着相关数据随时可能发布。据吉利德试验方案,两项临床试验将于5月结束,目前尚未有其他数据发布。
美国两家瑞德西韦临床试验基地的部分数据流出
据美国医疗新闻网站STAT 在4月16日报道,一项在美国芝加哥大学临床中心进行的瑞德西韦抗新冠肺炎临床试验中,125例新冠患者在接受瑞德西韦治疗后,大部分在6天内即治愈出院,其中包括113例重症患者,死亡仅2例。医生在密切观察该药治疗效果发现,大多数患者“发烧和呼吸道症状迅速恢复”,一天后撤下呼吸机,不到一周就康复出院。吉利德并未确认STAT报道的研究数据是否属于其试验的一部分,但根据美国临床试验数据库,美国芝加哥大学是其中一个临床中心。
解读:(1)这是全球首份关于瑞德西韦治疗新冠肺炎的单中心3期临床试验初步结果报道,确实其疗效令人鼓舞。该研究与4月10日《新英格兰医学杂志》刊发的瑞德西韦治疗重症新冠肺炎患者的研究有两个重要区别:一是该研究不是基于同情用药条件下做的观察,而是一项正式的临床试验,因此对于病例的招募条件更严格,数据也更为可靠,证据级别更高。二是该研究纳入的病例数量更多,共有125例,而后者仅53例,病例数量越多当然研究结果也更为可靠。(2)不过,依然要客观地认识到,该研究并没有设置对照组,属于单臂临床试验,患者康复尚不能直接归因于瑞德西韦的作用,且病例数量仍相对有限,从统计学角度也不足以确定瑞德西韦作为新冠肺炎治疗药物的安全性和有效性。评价一个新药研发成功的最终金标准是大规模多中心随机安慰剂对照双盲临床试验,因此还需等待更多高质量的临床试验数据的披露。(3)总的来说,该临床试验大大增加了瑞德西韦成为治疗新冠肺炎特效药的潜力,值得高度期待。
2020年4月21日,消息称美国另一家医院临床试验初步显示有效。USNews网站报道,美国休斯敦卫理公会医院研究人员报告称,两项使用抗病毒药物于瑞德西韦治疗COVID-19患者的临床试验初步数据令人鼓舞。休斯敦卫理公会医院是美国第5家加入的瑞德西韦临床试验基地,于3月中旬开始招募治疗患者。中症患者接受于瑞德西韦治疗5天或10天,而重症患者则接受该药物治疗10天。自3月23日以来,他们已经用这种药物治疗了41名大多数是重症的患者,目前没有一例病人死亡,一半人已出院。还有迹象表明,瑞德西韦可能可以避免病情加重而使用呼吸机。
美国NIAID发起的双盲对照临床试验重症组数据有望于本月底前公布
美国国家过敏和传染病研究所(NIAID)于2月21日发起一项瑞德西韦双盲对照临床试验,该试验将随机分配患者使用瑞德西韦或安慰剂,以对照比较试验结果。该试验正在入组约800名具有不同症状的患者,重症组数据有望于本月底前公布,中轻症组的数据有望于5月下旬公布。
正在进行临床试验汇总
目前仍有4项瑞德西韦临床试验正在进行中,包括吉利德科学牵头两项针对普通症和重症的临床试验,美国国家过敏症和传染病研究所(NIAID)于2月21日开启的全球试验,以及WHO开启的“团结试验”。整理相关媒体报道的信息,汇总相应进度见下表。也就是说4月还会有3项研究结果会陆续公布,大概率会是好消息。
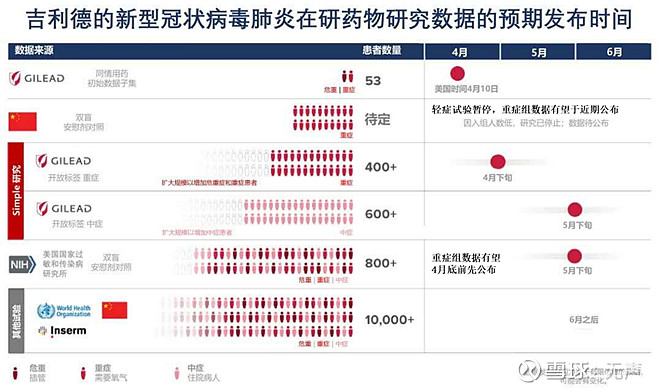
瑞德西韦在恒河猴试验中被证明有明显效果
当地时间4月15日,美国国家过敏症和传染病研究所(NIAID)病毒学家Emmie团队等人在预印本平台bioRxiv发布了一篇研究,指出与对照组相比,用瑞德西韦治疗的恒河猴呼吸道症状和肺部炎症明显减少,肺部病毒载量也显著降低。这项研究意义重大,因为这是全球首个在与人类最为接近的动物模型恒河猴中开展的瑞德西韦治疗新冠肺炎空白对照试验,用药各项关键指标都出现明显改善,增加了更有力的证据。

4月4日吉利德公司董事长公开信
吉利德现在的重要职责之一是确保瑞德西韦的充足供应。为临床试验、同情用药以及扩大可及方案提供药品,我们对供应量的提升实际上是从零开始的。迄今为止,我们在这方面取得的进展得益于我们自1月份以来采取的迅速扩大生产和增加可供应量的举措。当我们知道瑞德西韦可能具有治疗新型冠状病毒的潜力时,我们的团队随即开始建立了可实现大规模生产的供应链。在接下来的日子里,随着交货期较长的原材料到货可以用于生产,我们将能够进一步增加瑞德西韦的供应。我们设定了一个雄心勃勃的目标,力争到10月份生产超过可供50万个疗程使用的药品,到今年年底的可供应量要超过100万个疗程。为了帮助我们实现并超越这一目标,我们正在建立一个由制药和化学制造商组成的联盟,他们分布在全球各地,可以扩大原材料供应和生产的全球能力。这种合作方式可获得的成果远远超过我们任何一方单独工作所能取得的成就。瑞德西韦供应链的国际性提醒我们,各国必须共同努力,为世界创造足够的供应。$吉利德科学(GILD)$
4月10日吉利德公司新闻稿
“尽管在同情用药分析中观察到的结果令人鼓舞,但数据有限,” 吉利德科学公司首席医疗官,医学博士Merdad Parsey说。“吉利德目前正在开展瑞德西韦的多项临床研究,预计未来几周会有初步数据。我们的目标是尽快积累越来越多的证实数据,以更充分地评估瑞德西韦的潜力,并在恰当的情况下,支持该在研药物更广泛的应用。”
意外泄露的瑞德西韦中国临床试验结果并不能否定其潜在效果
北京时间4月24日凌晨,英国《金融时报》以及美国医学媒体 STAT 报道称,吉利德科学在中国开展的瑞德西韦试验结果被意外泄露在世界卫生组织(WHO)的网站上。摘要显示:237名患者参与了这项试验,使用了该药物的患者死亡率为13.9%,而接受标准治疗的患者死亡率为12.8%,实验结果表明瑞德西韦并没有改善新冠病毒感染的重症患者病情或减少血液中的病毒含量,且这种药也有明显的副作用。对于此次“意外泄漏”,世卫组织发言人随后表示,该实验的摘要未经审核,并不是最终报告,误发了研究报告,发现失误后就删除了报告。受此利空消息冲击,美股吉利德科学周四盘中一度跳水至8.35%,收跌4.3%。
解读:经查证多方资料综合分析,我认为国内重症患者临床试验的真实数据结果极大概率是偏中性的:从两组间比较,瑞德西韦治疗组和安慰剂对照组的临床效果的确没有统计学差异,而进一步细分亚组后,发病早期开始接受瑞德西韦治疗的病例有效率显著高于对照组,体现出疗效,而中晚期接受治疗的病例无效。也就是说该研究的最终结论估计是早期开始给予瑞德西韦抗病毒治疗是非常有必要的。而吉利德4月底即将公布的重症患者试验因为病例纳入标准要求确诊4天以内,其结果也更加值得高度期待。
总结:完全有理由审慎乐观了
虽然目前为止全球所有瑞德西韦治疗新冠肺炎的临床试验正式结果都还没公布,但当前已经得到的证据来看,包括国内中科院武汉病毒所开展的细胞实验、美国NIAID开展的恒河猴空白对照试验、《新英格兰医学杂志》发布的瑞德西韦同情用药回顾性分析结果、芝加哥大学医学院的125例单臂临床试验初步结果、休斯敦卫理公会医院试验基地传出的初步有效信号,均可以很好地互相印证,而意外泄露的中国临床试验结果也并不能否定瑞德西韦早期治疗的潜在效果,我觉得完全有理由审慎乐观了。全世界都在期待这个game changer,能够扭转这场百年一遇的大疫情,并有效避免全球经济危机,全球资本市场也有望迎来见底回升。危机危中有机,积极的人总是能从每一次危机中看到机会。伟大的公司,从来都是能够改变世界的,成功的投资,就是带着你的钱与改变世界的公司站在一起。我相信,当前也是A股这轮科技股大牛市的最后一次黄金坑,押注中国,押注科技创新,投资未来!